Métabolisme protéique global associé au vieillissement normal ou lié à une fragilité
Conférencier : Dr José Morais, M.D., FRCPC, service de gériatrie et Centre de nutrition et des sciences de l’alimentation de McGill, Université McGill, Montréal (Québec).
Le vieillissement est associé à des modifications qui pourraient affecter le métabo- lisme des protéines. Le Dr José Morais a parlé de ce métabolisme, en passant en revue des études comparant le métabolisme protéique des personnes âgées et des sujets plus jeunes.
La sarcopénie se définit par une perte de la masse et de la fonction musculaires. À tout moment, la quantité de masse musculaire dépend du taux de synthèse et de dégradation protéiques. Un déséquilibre entre ces deux phénomènes entraîne une augmentation ou une diminution de la masse corporelle maigre.
Les éléments physiologiques de base du métabolisme protéique montrent que les protéines sont essentielles à la structure et à la fonction cellulaires. Les protéines ne sont pas stockées; leur synthèse ou leur dégradation s’effectue selon un processus dynamique continu. Ce processus de renouvellement entraîne obligatoirement une perte d’azote, l’élément de base des acides aminés (éléments constitutifs des protéines). L’alimentation doit donc compenser cette perte d’azote et fournir notamment à l’organisme les acides aminés essentiels qu’il est incapable de synthétiser (Figure 1).
Normalement la réponse varie avec la dose, c’est-à-dire que l’équilibre entre l’apport en protéines et le taux de protéines dans l’organisme dépend de la consommation et de la qualité des protéines (reflétant la quantité d’acides aminés essentiels). La qualité des protéines et la quantité dont l’organisme a besoin sont également interdépendants.
Cependant, ces relations évoluent au cours de la vie. C’est un domaine que l’on connaît mal, notamment dans le contexte de la maladie.
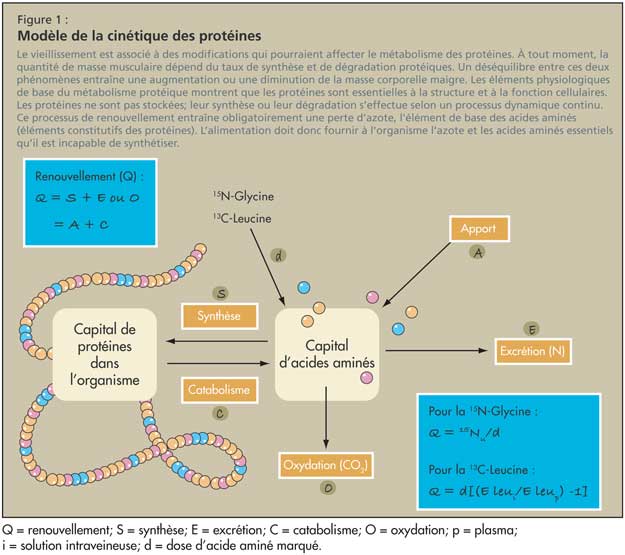
Modèle de la cinétique des protéines
Il est possible de mesurer le taux de renouvellement protéique (cinétique des protéines) à l’aide d’isotopes stables. En théorie, il existe un équilibre entre un capital d’acides aminés et un capital de protéines dans l’organisme. Le capital d’acides aminés est approvisionné par l’alimentation ou la dégradation des protéines dans l’organisme. Les acides aminés quittant ce capital sont utilisés pour la synthèse protéique ou sont dégradés. Les éléments dégradés peuvent être piégés dans l’air expiré.
L’IMC des personnes âgées indépendantes et en bonne santé peut être normal (IMC : 23-25), mais avec l’âge l’adiposité augmente et le taux de tissu maigre diminue. Des études portant sur la cinétique des protéines ont montré que le renouvellement protéique par kg de poids corporel est moins rapide chez les personnes âgées que chez les sujets plus jeunes. Cependant, les observations du Dr Morais ont montré que le taux de renouvellement protéique exprimé par kg de masse corporelle maigre n’est pas affecté par le vieillissement, bien que cela n’exclue pas des modifications au niveau musculaire.
Pour évaluer l’effet de l’âge sur le taux de renouvellement protéique dans l’organisme, le Dr Morais et ses collègues ont comparé des images du corps entier de sujets jeunes et âgés, obtenues par IRM, et examiné les images au niveau de la mi-cuisse et de l’abdomen1. Les résultats ont montré que le taux d’infiltration graisseuse était beaucoup plus important chez les sujets âgés, notamment chez les personnes montrant une adiposité abdominale.
Dans un sous-groupe de patients, ils ont trouvé que les sujets âgés avaient une masse maigre et une masse musculaire moins importantes. Une analyse d’urine sur 24 heures a permis de mesurer la dégradation des protéines musculaires, estimée d’après le taux de 3-méthylhistidine, comme indice de catabolisme musculaire. Les résultats ont montré que les muscles des personnes âgées contribuaient moins au catabolisme protéique (25,8 % contre 38,4 %, p < 0,001). Toutes les mesures furent corrigées pour la masse corporelle maigre.
Le Dr Morais en a conclu que la baisse du taux de cinétique des protéines par kg de poids corporel chez les personnes âgées était due à une perte de tissu maigre. De plus, il a trouvé que les muscles des personnes âgées contribuaient moins au catabolisme protéique global, en raison de la diminution de la masse musculaire et du ralentissement du catabolisme fractionnel. Les muscles des personnes âgées sont moins actifs, moins forts et en moins bonne santé en raison des restrictions alimentaires en matière de protéines. De plus, il a souligné que l’organisme en état de stress a besoin de plus de protéines que d’habitude pour se remettre de troubles comme une infection ou un traumatisme.
Le Dr Morais a fait observer que certaines nouvelles données sont discordantes. Une étude menée par Short K et ses collègues sur la cinétique protéique globale post-absorption a comparé l’effet d’un programme d’exercice d’aérobie ou d’un programme de renforcement musculaire sur la composition corporelle2. Les résultats de cette étude ont montré que le vieillissement est associé à une diminution importante du renouvellement protéique et à un déclin progressif des processus de remaniement de l’organisme. Cependant, quel que soit l’âge, l’exercice entraînait une augmentation de la synthèse et de la performance des protéines musculaires. La synthèse de protéines musculaires augmentait de 22 % (p < 0,05), tant chez les personnes âgées que chez les sujets plus jeunes.
Fragilité
Au cours de ses recherches sur les personnes âgées, le Dr Morais a observé qu’une importante atrophie musculaire est associée à une fragilité. Une étude portant sur la cinétique globale des protéines et la dégradation des protéines musculaires a comparé 8 femmes âgées fragiles à 8 femmes âgées en bonne santé soumises à un régime alimentaire iso-énergétique et isoazoté pendant 9 jours3. À la fin de cette période, ils ont étudié les effets, chez les sujets fragiles, d’une supplémentation protéique permettant d’égaler la consommation protéique du groupe en bonne santé, sans en augmenter l’énergie.
Le régime alimentaire riche en protéines entraînait une augmentation du taux de protéines endogènes et un bilan azoté positif à la fin de la période de régime.
Le Dr Morais a déclaré que l’augmentation du catabolisme des protéines musculaires associée à la fragilité pourrait être un mécanisme d’accommodation par lequel le muscle fournit des acides aminés pour maintenir la masse et la fonction des organes viscéraux, indispensable à la survie, aux dépens de la masse musculaire. Les femmes fragiles de l’étude maintenaient leur aptitude à conserver l’azote lorsqu’elles consommaient plus de protéines. Un tel régime alimentaire pourrait entraîner des bienfaits en matière de santé, si le régime est suivi pendant suffisamment longtemps pour occasionner une augmentation du tissu maigre.
Sensibilité à l’insuline et vieillissement
Le Dr Morais a discuté de la résistance au métabolisme protéique. La synthèse des protéines est régulée par l’insuline (qui possède des récepteurs sur les cellules musculaires) : à jeun, l’insuline réduit la dégradation des protéines, alors qu’après un repas elle stimule la synthèse des protéines tant que le substrat est présent en quantité suffisante. Une carence en insuline ou une résistance à l’action de l’insuline entraîne un déficit protéique, une perte protéique et une sarcopénie.
Cependant, les données probantes en faveur d’un lien entre l’âge et la résistance à l’insuline sont discordantes. Une étude a fait appel à des épreuves de clamp hyperglycémique pour examiner la relation entre l’action de l’insuline et le vieillissement. Les résultats de cette étude ont montré que l’âge en tant que tel n’est pas une cause importante de résistance à l’insuline4. Pour l’ensemble du groupe d’étude, l’action de l’insuline diminuait légèrement avec l’âge, mais après cor- rection pour l’IMC cette relation n’était plus statistiquement significative. Une diminution importante avec l’âge de l’action de l’insuline, corrigée pour l’IMC, ne s’observait que chez les femmes minces (IMC < 25 kg/m2), dont la masse adipeuse augmentait également avec l’âge (augmentation de 0,38 % du poids corporel par décennie; p = 0,0007).
D’autres études sont en accord avec l’hypothèse qu’un déclin lié à l’âge de la fonction mitochondriale contribue à la résistance à l’insuline chez les personnes âgées. Le Dr Morais a discuté d’une étude par Petersen KF et ses collègues, qui a comparé la composition corporelle de sujets jeunes et âgés en essayant d’éliminer le facteur d’adiposité5. Les chercheurs ont trouvé que le vieillissement était associé à une accumulation de graisse dans les tissus musculaire et hépatique, due à un déclin de la fonction mitochondriale et à une altération de l’oxydation et de la phosphorylation.
Anabolisme des protéines musculaires et effets de l’insuline
Volpi et ses collègues ont mené une étude mesurant la synthèse et la dégradation des protéines musculaires, ainsi que le transport des acides aminés. Ils ont trouvé que l’anabolisme des protéines musculaires est stimulé par une absorption orale d’acides aminés et de glucose chez les personnes jeunes et âgées, bien que les sujets plus jeunes eussent un meilleur taux de rétention protéique6. Le Dr Morais a attribué ces bienfaits, observés chez les personnes jeunes, à l’action de l’insuline.
Le Dr Morais et ses collègues ont testé l’hypothèse que l’hyperinsulinémie stimule la synthèse protéique lorsque les concentrations post-absorption des acides aminés dans le plasma restent constantes7. Les sujets étudiés étaient des personnes âgées ou plus jeunes (les personnes âgées avaient toutes un bon profil en matière d’AVQ et l’ensemble des sujets, tous âges confondus, avait un IMC entre 22 et 26 et faisait preuve d’un équilibre azoté). Par rapport aux personnes âgées, les taux de perfusion du glucose étaient supérieurs chez les personnes jeunes. Les sujets plus jeunes présentaient également un taux plus important de renouvellement et de synthèse protéique. La dégradation des protéines était inhibée de façon similaire dans les deux groupes.
Une réduction de la masse maigre absolue et une augmentation de l’adiposité sont deux phénomènes associés à une modification de l’action anabolique de l’insuline. Ainsi, en matière de résistance à l’insuline, l’adiposité est plus importante que l’âge. De plus, la réponse anabolique de l’organisme à une hyperinsulinémie diminue avec l’âge, et d’autant plus chez les femmes que chez les hommes. Cette réponse émoussée des personnes âgées s’explique par l’incapacité de l’insuline à stimuler la synthèse protéique. Étant donné que les acides aminés sont capables de stimuler la synthèse protéique, les personnes âgées pourraient bénéficier d’un apport alimentaire plus riche en protéines, pour compenser la résistance à l’insuline associée au vieillissement.
Conclusion
Le Dr Morais a conclu en disant que le vieillissement est partiellement respon-sable de la sarcopénie. Des lésions de l’ADN mitochondrial entraînent un déclin fonctionnel et une diminution de la production énergétique et de la capa-cité à synthétiser des protéines musculaires. Lorsque la fonction mitochondriale est ralentie, l’énergie va s’accumuler au lieu d’être utilisée normalement, ce qui va conduire à des infiltrations graisseuses dans le muscle, une cause bien connue de résistance à l’insuline. La diminution de la synthèse des protéines musculaires en tant que telle va entraîner une sarcopénie, qui est aggravée par une malnutrition.
Une fois la sarcopénie installée, la dépense énergétique est moindre, entraînant une adiposité et, en fin de compte, une résistance à l’insuline, cette dernière étant exacerbée par l’inactivité. Tous ces facteurs contribuent à une explication métabolique du processus sarcopénique lié au vieillissement.
Bibliographie
-
Morais JA, Ross R, Gougeon R et al. Distribution of protein turnover changes with age in humans as assessed by whole-body magnetic resonance image analysis to quantify tissue volumes. J Nutr 2000;130:784-91.
-
Short KR, Vittone JL, Bigelow ML, et al. Age and aerobic exercise training effects on whole body and muscle protein metabolism Am J Physiol Endocrinol Metab 2004;286:E92-101.
-
Chevalier S, Gougeon R, Nayar K, et al. Frailty amplifies the effects of aging on protein metabolism: role of protein intake. Am J Clin Nutr 2003;78:422-9.
-
Ferrannini E, Vichi S, Beck-Nielsen H, et al. Insulin action and age. Diabetes 1996;45:947-53.
-
Petersen KF, Befroy D, Dufour S, et al. Mitochondrial dysfunction in the elderly: possible role in insulin resistance. Science 2003;300:1140-2.
-
Volpi E, Mittendorfer B, Wolf SE, et al. Oral amino acids stimulate muscle protein anabolism in the elderly despite higher first-pass splanchnic extraction. Am J Physiol 1999;277(3 Pt 1):E513-20.
-
Chevalier S, Gougeon R, Choong N, et al. Influence of adiposity in the blunted whole-body protein anabolic response to insulin with aging. J Gerontol A Biol Sci Med Sci 2006;61:156-64.